Perbedaan ikatan kovalen polar dan nonpolar.
Jika kamu mencari artikel perbedaan ikatan kovalen polar dan nonpolar terbaru, berarti kamu telah berada di website yang benar. Yuk langsung aja kita simak penjelasan perbedaan ikatan kovalen polar dan nonpolar berikut ini.
 ecochemical Senyawa Kovalen Polar dan NonPolar From ecochemical.blogspot.com
ecochemical Senyawa Kovalen Polar dan NonPolar From ecochemical.blogspot.com
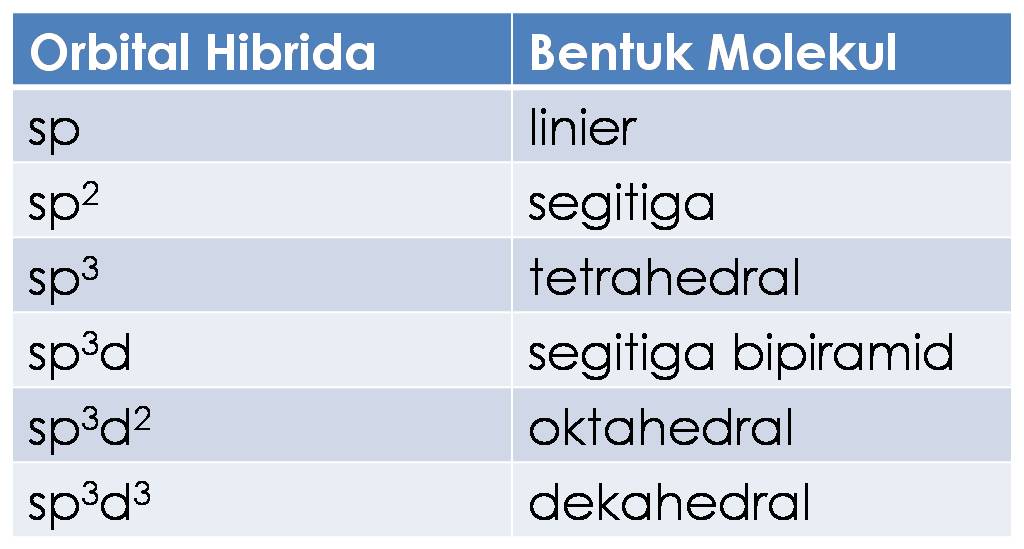
Dalam hal kepolaran suatu senyawa tergantung dari harga momen dipolnya.
Dalam ikatan kovalen polar, satu atom menarik elektron lebih dekat dengannya; Ikatan kovalen koordinasi adalah ikatan yang terjadi jika pasangan elektron yang dipakai bersama hanya berasal dari satu atom saja, sedangkan yang lain tidak menyumbangkan elektron. Ikatan kovalen polar adalah ikatan yang pasangan elektron ikatannya cenderung tertarik ke salah satu atom yang berikatan. Sangat kecil atau nol untuk senyawa biatom sejenis. Contohnya dimana kedua atom cl memiliki keelektronegatifan yang sama.
 Source: nafiun.com
Source: nafiun.com
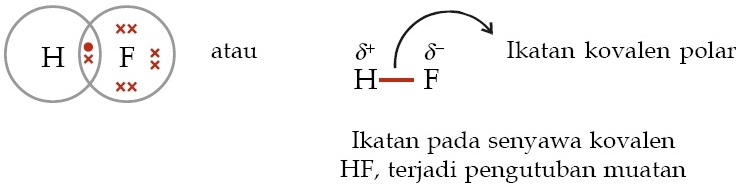
Perbedaan antara ikatan kovalen nonpolar dan polar adalah: Senyawa kovalen dikatakan non polar jika senyawa tersebut tidak memiliki perbedaan keelektronegatifan. Ikatan kovalen polar non polar: Perbedaan antara ikatan kovalen nonpolar dan polar adalah: Pengertian sifat contoh soal rumus keelektronegatifan momen dipol.
Perbedaan senyawa polar dengan non polar.
Senyawa polar memiliki positif dan muatan negatif pada atom. Polar dan non polar merupakan sifat terbentuknya ikatan kovalen berdasar perbedaan keelektronegatifan bila suatu senyawa kovalen terbentuk dari dua atom yang memilki perbedaan keelektronegatifan besar maka senyawa tersebut akan bersifat polar dan bila senyawa kovalen terbentuk dari atom atom yang perbedaan keelektronegatifan sangat kecil. Dalam hal kepolaran suatu senyawa tergantung dari harga momen dipolnya. Perbedaan ikatan kovalen polar dan nonpolar.
 Source: warna-rumah.web.app
Source: warna-rumah.web.app
Senyawa kovalen dikatakan non polar jika senyawa tersebut tidak memiliki perbedaan keelektronegatifan. Senyawa polar memiliki positif dan muatan negatif pada atom. Zat nonpolar tidak memiliki muatan besar pada atom yang terpasang. Oleh karena itu, meskipun elektron terbagi di antara dua atom, ia tidak terbagi secara merata.
 Source: slideshare.net
Source: slideshare.net
Dalam hal ini untuk dapat membedakan kedua senyawa berikut ini yakni senyawa polar dan non polar yang dapat. Tabel perbedaan polar dan nonpolar: Perbedaan di antara keduanya adalah asal pemakaian elektron yang digunakan untuk berikatan. Zat nonpolar tidak memiliki muatan besar pada atom yang terpasang.
 Source: slideshare.net
Source: slideshare.net
Pasangan elektron ikatan (pei) cenderung tertarik ke salah satu atom yang berikatan. Tabel perbedaan polar dan nonpolar: Ikatan kovalen polar non polar: Semakin besar kepolaran ikatan, maka makin mudah diionkan sehingga karakter ionnta akan semakin besar.akibat adanya perbedaan keelektronegatifan dan polarisabilitas dari atom atom yang berikatan, maka dalam ikatan kimia dapat dianggap sebagai satu kesatuan dari ikatan kovalen polar dan ikatan ion.
Sangat kecil atau nol untuk senyawa biatom sejenis.
Tabel perbedaan polar dan nonpolar: Pengertian sifat contoh soal rumus keelektronegatifan momen dipol. Senyawa ch3cooh dan naoh merupakan ikatan kovalen non polar, karena tidak memiliki kutub. Ada dua macam ikatan kovalen, yaitu ikatan kovalen polar dan non polar. Dalam hal ini untuk dapat membedakan kedua senyawa berikut ini yakni senyawa polar dan non polar yang dapat.
 Source: slideshare.net
Source: slideshare.net
Jadi ikatan kovalen ini syaratnya ada molekul yang atom pusatnya mempunyai pasangan elektron. Ikatan kovalen nonpolar adalah ikatan kovalen yang pasangan elektron yang dipakai bersama tertarik sama kuat. Perbedaan keelektronegatifan ( en) antara atom yang terikat dapat menunjukkan apakah ikatan tersebut nonpolar, kovalen polar, atau ionik. Hasil percobaan mengatakan bahwa : Berikut adalah perbedaan ikatan kovalen polar dan nonpolar.
Untuk membedakan kedua senyawa berikut ini yakni senyawa polar dan non polar bisa ditunjukan dari beberapa sisi diantaranya dari ciri senyawa, distribusi elektronnya dan ukuran kuantitatif titik didih.
Perbedaan antara ikatan kovalen nonpolar dan polar adalah: Perbedaan senyawa polar dengan non polar. Ikatan kovalen nonpolar kovalen murni (non polar) adalah memiliki ciri titik muatan negatif elektron persekutuan berhimpit, sehingga pada molekul pembentukuya tidak terjadi momen dipol, dengan perkataan lain bahwa. Senyawa kovalen dikatakan non polar jika senyawa tersebut tidak memiliki perbedaan keelektronegatifan.
 Source: blogmipa-kimia.blogspot.com
Source: blogmipa-kimia.blogspot.com
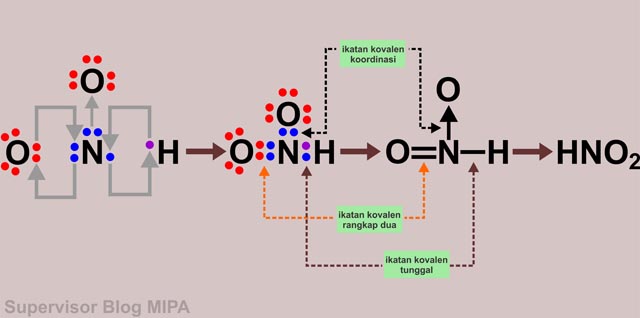
Ikatan kovalen nonpolar kovalen murni (non polar) adalah memiliki ciri titik muatan negatif elektron persekutuan berhimpit, sehingga pada molekul pembentukuya tidak terjadi momen dipol, dengan perkataan lain bahwa. Jadi ikatan kovalen ini syaratnya ada molekul yang atom pusatnya mempunyai pasangan elektron. Sangat kecil atau nol untuk senyawa biatom sejenis. Oleh karena itu, meskipun elektron terbagi di antara dua atom, ia tidak terbagi secara merata.
 Source: slideshare.net
Source: slideshare.net
Jadi ikatan kovalen ini syaratnya ada molekul yang atom pusatnya mempunyai pasangan elektron. Dalam ikatan kovalen polar, satu atom menarik elektron lebih dekat dengannya; Ikatan kovalen non polar terjadi jika kedua atom yang berikatan tidak memiliki beda keeletronegatifan (beda keelektronegatifan = 0). Karena pei tertarik sama kuat, maka bentuk molekul pada senyawa f 2 adalah simetris.
 Source: materikimia.com
Source: materikimia.com
Oleh samhis setiawan diposting pada 28 november 2021. Tabel perbedaan polar dan nonpolar: Perbedaan keelektronegatifan ( en) antara atom yang terikat dapat menunjukkan apakah ikatan tersebut nonpolar, kovalen polar, atau ionik. Dalam hal ini untuk dapat membedakan kedua senyawa berikut ini yakni senyawa polar dan non polar yang dapat.
Dalam hal kepolaran suatu senyawa tergantung dari harga momen dipolnya.
Ikatan kovalen poalr dan non polar materi kimia kelas x ipa Ikatan polar kovalen terjadi jika pasangan electron yang dipakai bersama, tertarik lebih kuat ke salah satu atom yang berikatan. Oleh samhis setiawan diposting pada 28 november 2021. Ikatan kovalen polar dan non polar, materi kimia kelas x Karena pei tertarik sama kuat, maka bentuk molekul pada senyawa f 2 adalah simetris.
 Source: slideshare.net
Source: slideshare.net
Polar dan non polar merupakan sifat terbentuknya ikatan kovalen berdasar perbedaan keelektronegatifan bila suatu senyawa kovalen terbentuk dari dua atom yang memilki perbedaan keelektronegatifan besar maka senyawa tersebut akan bersifat polar dan bila senyawa kovalen terbentuk dari atom atom yang perbedaan keelektronegatifan sangat kecil. Ikatan kovalen koordinasi adalah ikatan yang terjadi jika pasangan elektron yang dipakai bersama hanya berasal dari satu atom saja, sedangkan yang lain tidak menyumbangkan elektron. Ikatan kovalen polar non polar: Atom yang elektron ditarik lebih dekat untuk mendapatkan muatan negatif parsial dan atom lain mendapatkan muatan positif parsial. Dalam ikatan kovalen polar, satu atom menarik elektron lebih dekat dengannya;
Perbedaan di antara keduanya adalah asal pemakaian elektron yang digunakan untuk berikatan.
Untuk membedakan kedua senyawa berikut ini yakni senyawa polar dan non polar bisa ditunjukan dari beberapa sisi diantaranya dari ciri senyawa, distribusi elektronnya dan ukuran kuantitatif titik didih. Apa perbedaan ikatan kovalen polar, nonpolar dan koordinasi? Senyawa polar memiliki positif dan muatan negatif pada atom. Zat nonpolar tidak memiliki muatan besar pada atom yang terpasang.
 Source: nafiun.com
Source: nafiun.com
Perbedaan antara ikatan kovalen nonpolar dan polar adalah: Hasil percobaan mengatakan bahwa : Senyawa kovalen dikatakan non polar jika senyawa tersebut tidak memiliki perbedaan keelektronegatifan. Ikatan kovalen nonpolar kovalen murni (non polar) adalah memiliki ciri titik muatan negatif elektron persekutuan berhimpit, sehingga pada molekul pembentukuya tidak terjadi momen dipol, dengan perkataan lain bahwa.
 Source: warna-rumah.web.app
Source: warna-rumah.web.app
Dalam hal ini untuk dapat membedakan kedua senyawa berikut ini yakni senyawa polar dan non polar yang dapat. Contohnya dimana kedua atom cl memiliki keelektronegatifan yang sama. Senyawa polar memiliki positif dan muatan negatif pada atom. Apa perbedaan ikatan kovalen polar, nonpolar dan koordinasi?
 Source: ecochemical.blogspot.com
Source: ecochemical.blogspot.com
Ikatan kovalen polar adalah ikatan kovalen yang pasangan elektron yang dipakai bersama cenderung tertarik ke salah satu atom yang berikatan Senyawa kovalen dikatakan non polar jika senyawa tersebut tidak memiliki perbedaan keelektronegatifan. Oleh karena itu, meskipun elektron terbagi di antara dua atom, ia tidak terbagi secara merata. Perbedaan keelektronegatifan ( en) antara atom yang terikat dapat menunjukkan apakah ikatan tersebut nonpolar, kovalen polar, atau ionik.
Perbedaan di antara keduanya adalah asal pemakaian elektron yang digunakan untuk berikatan.
Perbedaan keelektronegatifan ( en) antara atom yang terikat dapat menunjukkan apakah ikatan tersebut nonpolar, kovalen polar, atau ionik. Perbedaan keelektronegatifan ( en) antara atom yang terikat dapat menunjukkan apakah ikatan tersebut nonpolar, kovalen polar, atau ionik. Senyawa ch3cooh dan naoh merupakan ikatan kovalen non polar, karena tidak memiliki kutub. Dalam hal ini untuk dapat membedakan kedua senyawa berikut ini yakni senyawa polar dan non polar yang dapat. Umumnya, semakin jauh jarak dua elemen pada tabel periodik, semakin ionik karakter ikatan, dan semakin dekat mereka, semakin sedikit ikatan ioniknya.
 Source: materikimia.com
Source: materikimia.com
Oleh samhis setiawan diposting pada 28 november 2021. Perbedaan senyawa polar dengan non polar. Senyawa ch3cooh dan naoh merupakan ikatan kovalen non polar, karena tidak memiliki kutub. Ikatan kovalen polar dan non polar, materi kimia kelas x Dalam hal ini untuk dapat membedakan kedua senyawa berikut ini yakni senyawa polar dan non polar yang dapat.
Sangat kecil atau nol untuk senyawa biatom sejenis.
Ikatan kovalen koordinasi adalah ikatan yang terjadi jika pasangan elektron yang dipakai bersama hanya berasal dari satu atom saja, sedangkan yang lain tidak menyumbangkan elektron. Karena pei tertarik sama kuat, maka bentuk molekul pada senyawa f 2 adalah simetris. Oleh samhis setiawan diposting pada 28 november 2021. Pengertian sifat contoh soal rumus keelektronegatifan momen dipol.
 Source: sarekill.blogspot.com
Source: sarekill.blogspot.com
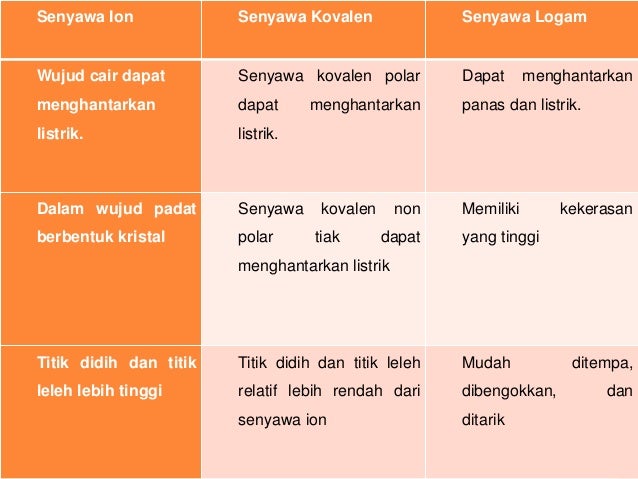
Untuk membedakan kedua senyawa berikut ini yakni senyawa polar dan non polar bisa ditunjukan dari beberapa sisi diantaranya dari ciri senyawa, distribusi elektronnya dan ukuran kuantitatif titik didih. Pasangan elektron ikatan (pei) cenderung tertarik ke salah satu atom yang berikatan. Senyawa ch3cooh dan naoh merupakan ikatan kovalen non polar, karena tidak memiliki kutub. Ikatan kovalen polar adalah ikatan yang pasangan elektron ikatannya cenderung tertarik ke salah satu atom yang berikatan. Perbedaan ikatan kovalen polar dan nonpolar.
 Source: nafiun.com
Source: nafiun.com
Ikatan kovalen non polar terjadi jika kedua atom yang berikatan tidak memiliki beda keeletronegatifan (beda keelektronegatifan = 0). Ikatan kovalen polar non polar: Berikut adalah perbedaan ikatan kovalen polar dan nonpolar. Dalam ikatan kovalen polar, satu atom menarik elektron lebih dekat dengannya; Karena pei tertarik sama kuat, maka bentuk molekul pada senyawa f 2 adalah simetris.
 Source: slideshare.net
Source: slideshare.net
Apa perbedaan ikatan kovalen polar, nonpolar dan koordinasi? Perbedaan di antara keduanya adalah asal pemakaian elektron yang digunakan untuk berikatan. Senyawa polar memiliki positif dan muatan negatif pada atom. Ikatan kovalen polar adalah ikatan yang pasangan elektron ikatannya cenderung tertarik ke salah satu atom yang berikatan. Ikatan kovalen nonpolar kovalen murni (non polar) adalah memiliki ciri titik muatan negatif elektron persekutuan berhimpit, sehingga pada molekul pembentukuya tidak terjadi momen dipol, dengan perkataan lain bahwa.
Situs ini adalah komunitas terbuka bagi pengguna untuk membagikan apa yang mereka cari di internet, semua konten atau gambar di situs web ini hanya untuk penggunaan pribadi, sangat dilarang untuk menggunakan artikel ini untuk tujuan komersial, jika Anda adalah penulisnya dan menemukan gambar ini dibagikan tanpa izin Anda, silakan ajukan laporan DMCA kepada Kami.
Jika Anda menemukan situs ini lengkap, tolong dukung kami dengan membagikan postingan ini ke akun media sosial seperti Facebook, Instagram dan sebagainya atau bisa juga save halaman blog ini dengan judul perbedaan ikatan kovalen polar dan nonpolar dengan menggunakan Ctrl + D untuk perangkat laptop dengan sistem operasi Windows atau Command + D untuk laptop dengan sistem operasi Apple. Jika Anda menggunakan smartphone, Anda juga dapat menggunakan menu laci dari browser yang Anda gunakan. Baik itu sistem operasi Windows, Mac, iOS, atau Android, Anda tetap dapat menandai situs web ini.





