Konfigurasi elektron k l m n.
Jika kamu mencari artikel konfigurasi elektron k l m n terbaru, berarti kamu telah berada di website yang benar. Yuk langsung saja kita simak pembahasan konfigurasi elektron k l m n berikut ini.
 KONFIGURASI ELEKTRON DAN ELEKTRON VALENSI Sady's Zone From sadyzone.blogspot.com
KONFIGURASI ELEKTRON DAN ELEKTRON VALENSI Sady's Zone From sadyzone.blogspot.com
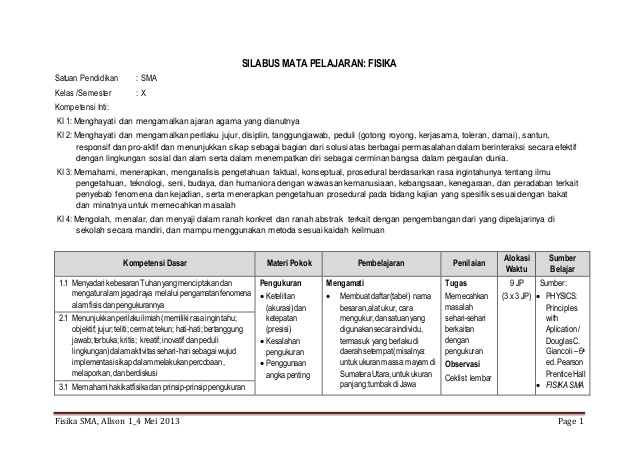
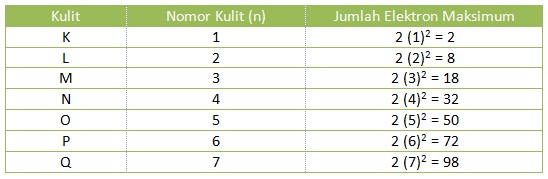
Kulit k maksimum berisi 2 elektron kulit l maksimum berisi 8 elektron kulit m maksimum berisi 18 elektron kulit n maksimum berisi 32 elektron kulit o maksimum berisi 50 elektron dst.
Bilangan kuantum utama (primer) digunakan untuk menyatakan tingkat energi utama yang dimiliki oleh elektron dalam sebuah atom. Ni (z = 28) : Elektron pita ini kita isikan seluruhnya pada kulit n. Kulit k (n=1) maksimum menampung elektron 2×1 2 =2. Tuliskan konfigurasi elektron pada atom tersebut!
 Source: rumuskimia.net
Source: rumuskimia.net
Kulit keempat (kulit n) = 32 elektron. Elektron pita ini kita isikan seluruhnya pada kulit n. Kulit pertama (kulit k) = 2 elektron. Bilangan kuantum utama (primer) digunakan untuk menyatakan tingkat energi utama yang dimiliki oleh elektron dalam sebuah atom. Konfigurasi elektron terbagi menjadi dua, yaitu.
Masih sisa 7 elektron, berarti < 8, sisa elektron semuanya masuk kulit berikutnya.
Sisanya adalah 8 buah elektron. Berikut cara menuliskan konfigurasi elektron berdasarkan kulit atom. Untuk cara menentukan konfigurasi elektron, berikut merupakan penjabaran elektronnya: Isikan elektron ke dalam kulit atom sesuai daya tampung maksimumnya.
 Source: studiobelajar.com
Source: studiobelajar.com
1s 2 2s 2 2p 6 3s 2 3p 6 4s 2 3d 8 atau [ar] 4s 2 3d 8; Bilangan kuantum utama (n) yang menyatakan tingkat energi. K l m n 2 8 18 8 sampai pada kulit m sudah terpakai 28 elektron. Masih sisa 7 elektron, berarti < 8, sisa elektron semuanya masuk kulit berikutnya.
 Source: rumuskimia.net
Source: rumuskimia.net
Konfigurasi elektron terbagi menjadi dua, yaitu. Jangan lupa klik tombol subscribe, like, comment, dan share. Masih sisa 7 elektron, berarti < 8, sisa elektron semuanya masuk kulit berikutnya. Bilangan kuantum utama tidak pernah bernilai nol.
 Source: sadyzone.blogspot.com
Source: sadyzone.blogspot.com
Konfigurasi elektron terbagi menjadi dua, yaitu. Kulit k (n=1) maksimum menampung elektron 2×1 2 =2. Kulit keempat (kulit n) = 32 elektron. Ni (z = 28) :
Kulit k maksimum berisi 2 elektron kulit l maksimum berisi 8 elektron kulit m maksimum berisi 18 elektron kulit n maksimum berisi 32 elektron kulit o maksimum berisi 50 elektron dst.
Sisanya adalah 8 buah elektron. Tidak semua unsur dalam tabel periodik dapat ditentukan dengan mudah posisi dan. Berikut cara menuliskan konfigurasi elektron berdasarkan kulit atom. Ni (z = 28) b. Sebuah kulit elektron yaitu beberapa subkulit yang berbagi bilangan kuantum yang sama yaitu n (nomor sebelum angka dalam sebuah orbital).
 Source: brainly.co.id
Source: brainly.co.id
Bilangan kuantum utama tidak pernah bernilai nol. Untuk cara menentukan konfigurasi elektron, berikut merupakan penjabaran elektronnya: Kulit kedua (kulit l) = 8 elektron. Penyebaran ini memiliki pola susunan tertentu yang disebut dengan konfigurasi elektron. Mulai dari lintasan yang paling dekat dengan inti yaitu kulit k.
Konfigurasi elektron terbagi menjadi dua, yaitu.
Ni (z = 28) : Jangan lupa klik tombol subscribe, like, comment, dan share. Suatu unsur memiliki konfigurasi elektron, k =2, l = 8, m = 8, n = 6. Tidak semua unsur dalam tabel periodik dapat ditentukan dengan mudah posisi dan.
 Source: studiobelajar.com
Source: studiobelajar.com
Ni (z = 28) b. Masih sisa 7 elektron, berarti < 8, sisa elektron semuanya masuk kulit berikutnya. Penyebaran ini memiliki pola susunan tertentu yang disebut dengan konfigurasi elektron. Anomali konfigurasi elektron berdasarkan sebuah eksperimen, ditemukan bahwa aturan pada konfigurasi elektron seperti yang sudah disebutkan.
 Source: theinsidemag.com
Source: theinsidemag.com
Isikan elektron ke dalam kulit atom sesuai daya tampung maksimumnya. Sebuah kulit elektron yaitu beberapa subkulit yang berbagi bilangan kuantum yang sama yaitu n (nomor sebelum angka dalam sebuah orbital). Bilangan kuantum utama tidak pernah bernilai nol. Bilangan kuantum utama (n) yang menyatakan tingkat energi.
 Source: rumuskimia.net
Source: rumuskimia.net
Kulit ketiga (kulit m) = 18 elektron. Sebuah kulit elektron yaitu beberapa subkulit yang berbagi bilangan kuantum yang sama yaitu n (nomor sebelum angka dalam sebuah orbital). Kulit ketiga (kulit m) = 18 elektron. Kulit k (n=1) maksimum menampung elektron 2×1 2 =2.
Bilangan kuantum utama (n) yang menyatakan tingkat energi.
Tentukan konfigurasi elektron dan jumlah elektron dalam setiap kulit elektron atom unsur berikut. Bilangan kuantum utama dapat mempunyai nilai semua bilangan positif, yaitu 1,2,3,4 dan seterusnya. Isikan elektron ke dalam kulit atom sesuai daya tampung maksimumnya. Dukung kami dengan tidak mendownload videonya dan hanya menyaksikannya di youtube. Tidak semua unsur dalam tabel periodik dapat ditentukan dengan mudah posisi dan.
 Source: brainly.co.id
Source: brainly.co.id
Bilangan kuantum utama (primer) digunakan untuk menyatakan tingkat energi utama yang dimiliki oleh elektron dalam sebuah atom. Tuliskan konfigurasi elektron pada atom tersebut! Salah satu isotopnya memiliki 28 neutron, nomor atom dan nomor massa unsur tersebut adalah…. Kulit pertama (kulit k) = 2 elektron. Diketahui keempat bilangan kuantum elektron terakhir pada suatu konfigurasi unsur adalah, n= 3, l= 1, m= −1, s=1/ −2, maka nomor atom dari unsur tersebut adalah.
Tentukan konfigurasi elektron dan jumlah elektron dalam setiap kulit elektron atom unsur berikut.
Kemudian, jika kulit pertama (kulit k) sudah terisi penuh, elektron kemudian mengisi kulit tingkat berikutnya yaitu kulit l (kulit ke dua, n = 2), dan seterusnya Pengisisan elektron dimulai dari tingkat energi (kulit) yang paling rendah yaittu kulit k. Jangan lupa klik tombol subscribe, like, comment, dan share. Isikan elektron ke dalam kulit atom sesuai daya tampung maksimumnya.
 Source: theinsidemag.com
Source: theinsidemag.com
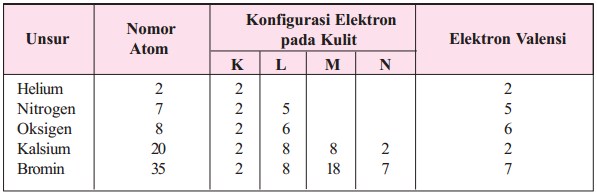
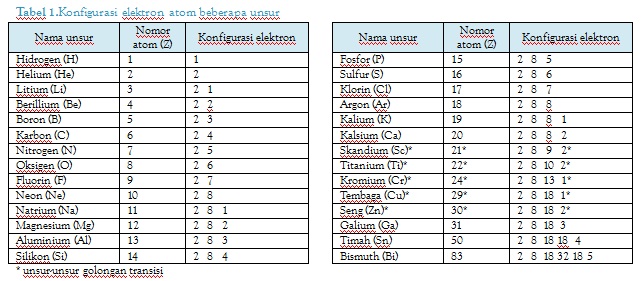
Menurut bohr, konfigurasi elektron adalah pengisian elektron yang dimulai dari tingkat energi (kulit) yang paling rendah, yaitu kulit k (kulit pertama, n = 1). Kulit kedua (kulit l) = 8 elektron. 3 li 4 be 5 b 6 c 7 n 8 o 9 f 10 ne 11 na 12 mg 13 al 14 si 15 p 16 s 17 cl 18 ar 19 k 20 ca 21 sc 22 ti 23 v 24 cr 25 mn 26 fe 27 co 28 ni 29 cu 30 zn 31 ga 32 ge 33 as 34 se 35 br 36 kr 52 te catatan awal: Sebuah kulit elektron yaitu beberapa subkulit yang berbagi bilangan kuantum yang sama yaitu n (nomor sebelum angka dalam sebuah orbital).
 Source: rumuskimia.net
Source: rumuskimia.net
Penyebaran ini memiliki pola susunan tertentu yang disebut dengan konfigurasi elektron. Jadi kulit terakhir dari unsur adalah n dengan jumlah elektron valensi = 8. Elektron pita ini kita isikan seluruhnya pada kulit n. Bilangan kuantum utama dapat mempunyai nilai semua bilangan positif, yaitu 1,2,3,4 dan seterusnya.
 Source: brainly.co.id
Source: brainly.co.id
Ni (z = 28) : Bilangan kuantum utama dapat mempunyai nilai semua bilangan positif, yaitu 1,2,3,4 dan seterusnya. Diketahui keempat bilangan kuantum elektron terakhir pada suatu konfigurasi unsur adalah, n= 3, l= 1, m= −1, s=1/ −2, maka nomor atom dari unsur tersebut adalah. Suatu unsur memiliki konfigurasi elektron, k =2, l = 8, m = 8, n = 6.
Menurut bohr, konfigurasi elektron adalah pengisian elektron yang dimulai dari tingkat energi (kulit) yang paling rendah, yaitu kulit k (kulit pertama, n = 1).
Bilangan kuantum utama tidak pernah bernilai nol. Kulit pertama (kulit k) = 2 elektron. K l m n 2 8 18 8 sampai pada kulit m sudah terpakai 28 elektron. Untuk cara menentukan konfigurasi elektron, berikut merupakan penjabaran elektronnya: Kemudian, jika kulit pertama (kulit k) sudah terisi penuh, elektron kemudian mengisi kulit tingkat berikutnya yaitu kulit l (kulit ke dua, n = 2), dan seterusnya
 Source: studiobelajar.com
Source: studiobelajar.com
Konfigurasi elektron pada unsur sr tersebut juga dapat ditulis [kr] 5s2dengan k=2, l=8, m=18, n=8, dan o=2. Kulit kedua (kulit l) = 8 elektron. Ni (z = 28) : Tentukan konfigurasi elektron dan jumlah elektron dalam setiap kulit elektron atom unsur berikut. Kemudian, jika kulit pertama (kulit k) sudah terisi penuh, elektron kemudian mengisi kulit tingkat berikutnya yaitu kulit l (kulit ke dua, n = 2), dan seterusnya
Diketahui keempat bilangan kuantum elektron terakhir pada suatu konfigurasi unsur adalah, n= 3, l= 1, m= −1, s=1/ −2, maka nomor atom dari unsur tersebut adalah.
Suatu unsur memiliki konfigurasi elektron, k =2, l = 8, m = 8, n = 6. Ni (z = 28) : Anomali konfigurasi elektron berdasarkan sebuah eksperimen, ditemukan bahwa aturan pada konfigurasi elektron seperti yang sudah disebutkan. Sisanya adalah 8 buah elektron.
 Source: sadyzone.blogspot.com
Source: sadyzone.blogspot.com
Kemudian, jika kulit pertama (kulit k) sudah terisi penuh, elektron kemudian mengisi kulit tingkat berikutnya yaitu kulit l (kulit ke dua, n = 2), dan seterusnya Anomali konfigurasi elektron berdasarkan sebuah eksperimen, ditemukan bahwa aturan pada konfigurasi elektron seperti yang sudah disebutkan. Jangan lupa klik tombol subscribe, like, comment, dan share. Kulit keempat (kulit n) = 32 elektron. Suatu unsur memiliki konfigurasi elektron, k =2, l = 8, m = 8, n = 6.
 Source: rumuskimia.net
Source: rumuskimia.net
Untuk cara menentukan konfigurasi elektron, berikut merupakan penjabaran elektronnya: Kulit k (n=1) maksimum menampung elektron 2×1 2 =2. Bilangan kuantum utama (primer) digunakan untuk menyatakan tingkat energi utama yang dimiliki oleh elektron dalam sebuah atom. Jadi kulit terakhir dari unsur adalah n dengan jumlah elektron valensi = 8. Menurut bohr, konfigurasi elektron adalah pengisian elektron yang dimulai dari tingkat energi (kulit) yang paling rendah, yaitu kulit k (kulit pertama, n = 1).
 Source: studiobelajar.com
Source: studiobelajar.com
Ni (z = 28) b. Kulit kedua (kulit l) = 8 elektron. Kulit keempat (kulit n) = 32 elektron. Berikut cara menuliskan konfigurasi elektron berdasarkan kulit atom. Tidak semua unsur dalam tabel periodik dapat ditentukan dengan mudah posisi dan.
Situs ini adalah komunitas terbuka bagi pengguna untuk berbagi apa yang mereka cari di internet, semua konten atau gambar di situs web ini hanya untuk penggunaan pribadi, sangat dilarang untuk menggunakan artikel ini untuk tujuan komersial, jika Anda adalah penulisnya dan menemukan gambar ini dibagikan tanpa izin Anda, silakan ajukan laporan DMCA kepada Kami.
Jika Anda menemukan situs ini bermanfaat, tolong dukung kami dengan membagikan postingan ini ke akun media sosial seperti Facebook, Instagram dan sebagainya atau bisa juga bookmark halaman blog ini dengan judul konfigurasi elektron k l m n dengan menggunakan Ctrl + D untuk perangkat laptop dengan sistem operasi Windows atau Command + D untuk laptop dengan sistem operasi Apple. Jika Anda menggunakan smartphone, Anda juga dapat menggunakan menu laci dari browser yang Anda gunakan. Baik itu sistem operasi Windows, Mac, iOS, atau Android, Anda tetap dapat menandai situs web ini.