Contoh reaksi redoks sebagai pelepasan dan penerimaan elektron.
Jika kamu sedang mencari artikel contoh reaksi redoks sebagai pelepasan dan penerimaan elektron terlengkap, berarti kamu telah berada di blog yang tepat. Yuk langsung aja kita simak ulasan contoh reaksi redoks sebagai pelepasan dan penerimaan elektron berikut ini.
 Carilah Masing-masing 2 Contoh Dari Reaksi Oksidasi Dan Reduksi Dengan Teori Pelepasan Dan - Brainlycoid From brainly.co.id
Carilah Masing-masing 2 Contoh Dari Reaksi Oksidasi Dan Reduksi Dengan Teori Pelepasan Dan - Brainlycoid From brainly.co.id
Reaksi redoks sebagai reaksi pelepasan dan pengikatan / penerimaan elektron 1).
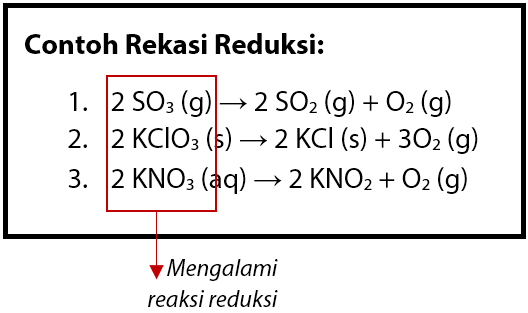
Reaksi di atas menunjukkan terjadinya pelepasan dan pengikatan elektron, maka dapat disimpulkan sebagai berikut. Berdasarkan gambar di atas : 4) so 3, kclo 3, kno 3. Nah, pada kesempatan kali ini kita akan membahas konsep reaksi redoks berdasarkan pengikatan dan pelepasan oksigen. Reaksi pengikatan atau penerimaan elektron.
 Source: brainly.co.id
Source: brainly.co.id
Kritik dan saran tentang redoks berdasarkan pelepasan dan penerimaan elektron dapat anda sampaikan melalui kotak komentar dibawah ini. Reaksi oksidasi dan reduksi ternyata bukan hanya melibatkan oksigen, melainkan juga melibatkan elektron. Suatu reaksi kimia dikatakan sebagai suatu reaksi redoks jika: Dalam konsep redoks, peristiwa pelepasan elektron dinamakan oksidasi, sedangkan peristiwa penerimaan elektron dinamakan reduksi. Oksidasi adalah peristiwa pelepasan elektron.
Terjadi pengikatan oksigen (oksidasi) dan pelepasan oksigen (reduksi).
Dalam konsep redoks, peristiwa pelepasan elektron dinamakan oksidasi, sedangkan peristiwa penerimaan elektron dinamakan reduksi. Berdasarkan gambar di atas : Oksidasi adalah peristiwa pengikatan oksigen adapun contoh yang terkait dengan reaksi oksidasi berdasarkan konsep ini adalah sebagai berikut: Konsep redoks berdasarkan pelepasan dan penerimaan elektron.
 Source: idschool.net
Source: idschool.net
Berdasarkan gambar di atas : Reaksi redoks sebagai reaksi pelepasan dan pengikatan / penerimaan elektron 1). Terjadi kenaikan bilangan oksidasi (oksidasi) dan penurunan bilangan oksidasi (reduksi) Terjadi pelepasan elektron (oksidasi) dan penerimaan elektron (reduksi).
 Source: kimiavegas.wordpress.com
Source: kimiavegas.wordpress.com
Reduksi adalah reaksi pengikatan atau penerimaan elektron. Terjadi kenaikan bilangan oksidasi (oksidasi) dan penurunan bilangan oksidasi (reduksi) Nah, seperti yang sudah dijelaskan sebelumnya, konsep reaksi redoks ini ada yang melibatkan pelepasan dan pengikatan oksigen, pelepasan dan pengikatan elektron, serta kenaikan dan penurunan bilangan oksidasi, ya.tentunya, kamu bisa pahami materi ini lebih. Konsep reaksi redoks berdasarkan pelepasan dan penerimaan elektron reaksi oksidasi dan reduksi ternyata bukan hanya melibatkan oksigen, melainkan juga melibatkan elektron.
 Source: materikimia.com
Source: materikimia.com
Reaksi redoks pada peristiwa perkaratan besi dapat dijelaskan dengan reaksi berikut: Terimakasih atas kunjungan anda pada blog ini. Terjadi kenaikan bilangan oksidasi (oksidasi) dan penurunan bilangan oksidasi (reduksi) Oksidator adalah zat yang menerima elektron.sedangkan reduktor adalah zat yang melepas.
Memang oksigen merupakan salah satu bahan yang dapat mengoksidasi zat lain yang berinteraksi dengannya.
Dalam konsep redoks, peristiwa pelepasan elektron dinamakan oksidasi, sedangkan peristiwa penerimaan elektron dinamakan reduksi. Adapun konfigurasi elektron atom cl adalah 2 8 7 sehingga elektron valensinya adalah 7. Dalam konsep redoks, peristiwa pelepasan elektron dinamakan oksidasi, sedangkan peristiwa penerimaan elektron dinamakan reduksi. Oksidasi adalah peristiwa pengikatan oksigen adapun contoh yang terkait dengan reaksi oksidasi berdasarkan konsep ini adalah sebagai berikut: Ca ca2+ + 2e reduksi :
 Source: idschool.net
Source: idschool.net
Konsep reaksi redoks berdasarkan pelepasan dan penerimaan elektron reaksi oksidasi dan reduksi ternyata bukan hanya melibatkan oksigen, melainkan juga melibatkan elektron. Contoh reaksi redoks pada industri. Konsep redoks berdasarkan pelepasan dan penerimaan elektron. Terimakasih atas kunjungan anda pada blog ini. Apa pengertian oksidasi, reduksi, reduktor dan oksidator berdasarkan pada penerimaan dan pelepasan electron, pahami contoh berikut!
Contoh reaksi redoks pada industri.
Nah, seperti yang sudah dijelaskan sebelumnya, konsep reaksi redoks ini ada yang melibatkan pelepasan dan pengikatan oksigen, pelepasan dan pengikatan elektron, serta kenaikan dan penurunan bilangan oksidasi, ya.tentunya, kamu bisa pahami materi ini lebih. 4) so 3, kclo 3, kno 3. Berdasarkan pengikatan dan pelepasan elektron. Contoh reaksi redoks pada industri.
 Source: kimiavegas.wordpress.com
Source: kimiavegas.wordpress.com
Oksidasi adalah peristiwa pelepasan elektron. Berdasarkan pengikatan dan pelepasan elektron. Apa pengertian oksidasi, reduksi, reduktor dan oksidator berdasarkan pada penerimaan dan pelepasan electron, pahami contoh berikut! Terimakasih atas kunjungan anda pada blog ini.
 Source: kimiavegas.wordpress.com
Source: kimiavegas.wordpress.com
Reaksi oksidasi pelepasan penerimaan elektron. Oksidasi adalah peristiwa pengikatan oksigen adapun contoh yang terkait dengan reaksi oksidasi berdasarkan konsep ini adalah sebagai berikut: Terjadi kenaikan bilangan oksidasi (oksidasi) dan penurunan bilangan oksidasi (reduksi) 1) hematit fe 2 o 3;
 Source: kimiavegas.wordpress.com
Source: kimiavegas.wordpress.com
- hematit fe 2 o 3; Reaksi di atas menunjukkan terjadinya pelepasan dan pengikatan elektron, maka dapat disimpulkan sebagai berikut. Reduksi adalah reaksi pengikatan atau penerimaan elektron. Adapun konfigurasi elektron atom cl adalah 2 8 7 sehingga elektron valensinya adalah 7.
Oksidasi adalah peristiwa pengikatan oksigen adapun contoh yang terkait dengan reaksi oksidasi berdasarkan konsep ini adalah sebagai berikut:
Besi berkarat, ataupun minyak goreng yang menjadi tengik merupakan contoh reaksi redoks yang melibatkan oksigen. 1) hematit fe 2 o 3; 4) so 3, kclo 3, kno 3. Reaksi oksidasi pelepasan penerimaan elektron. Apa pengertian oksidasi, reduksi, reduktor dan oksidator berdasarkan pada penerimaan dan pelepasan electron, pahami contoh berikut!
 Source: idschool.net
Source: idschool.net
Memang oksigen merupakan salah satu bahan yang dapat mengoksidasi zat lain yang berinteraksi dengannya. Kritik dan saran tentang redoks berdasarkan pelepasan dan penerimaan elektron dapat anda sampaikan melalui kotak komentar dibawah ini. Konsep redoks berdasarkan pelepasan dan pengikatan. 4) so 3, kclo 3, kno 3. Artikel redoks berdasarkan pelepasan dan penerimaan elektron ini ditulis oleh fauzan muhammad pada hari monday, january 7, 2013.
Konsep redoks berdasarkan pelepasan dan pengikatan.
Pada reaksi reduksi terjadi pelepasan oksigen. 4) so 3, kclo 3, kno 3. Oksidasi adalah peristiwa pengikatan oksigen adapun contoh yang terkait dengan reaksi oksidasi berdasarkan konsep ini adalah sebagai berikut: Ca ca2+ + 2e reduksi :
 Source: kimiavegas.wordpress.com
Source: kimiavegas.wordpress.com
Besi oksida dapat direduksi dengan cara direaksikan dengan gas hidrogen, persamaan reaksinya: Dalam konsep redoks, peristiwa pelepasan elektron dinamakan oksidasi, sedangkan peristiwa penerimaan elektron dinamakan reduksi. Konsep reaksi redoks berdasarkan pelepasan dan penerimaan elektron reaksi oksidasi dan reduksi ternyata bukan hanya melibatkan oksigen, melainkan juga melibatkan elektron. Terimakasih atas kunjungan anda pada blog ini.
 Source: tugassains.com
Source: tugassains.com
Konsep redoks berdasarkan pelepasan dan penerimaan elektron. Reaksi oksidasi dan reduksi ternyata bukan hanya melibatkan oksigen, melainkan juga melibatkan elektron. Reaksi redoks pada peristiwa perkaratan besi dapat dijelaskan dengan reaksi berikut: Contoh reaksi redoks pada industri.
 Source: idschool.net
Source: idschool.net
- perkaratan logam besi reaksi perkaratan logam besi: Berdasarkan pengikatan dan pelepasan elektron. Terimakasih atas kunjungan anda pada blog ini. Suatu reaksi kimia dikatakan sebagai suatu reaksi redoks jika:
Artikel redoks berdasarkan pelepasan dan penerimaan elektron ini ditulis oleh fauzan muhammad pada hari monday, january 7, 2013.
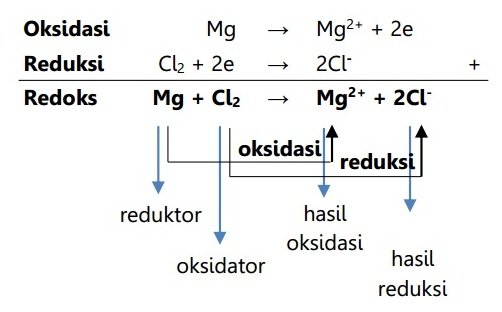
Apa pengertian oksidasi, reduksi, reduktor dan oksidator berdasarkan pada penerimaan dan pelepasan electron, pahami contoh berikut! Konsep redoks berdasarkan pelepasan dan penerimaan elektron. Ca ca2+ + 2e reduksi : Oksidator adalah zat yang menerima elektron.sedangkan reduktor adalah zat yang melepas. Reaksi redoks (gabungan oksidasi dan reduksi) oksidasi :
 Source: kimiavegas.wordpress.com
Source: kimiavegas.wordpress.com
Reaksi di atas menunjukkan terjadinya pelepasan dan pengikatan elektron, maka dapat disimpulkan sebagai berikut. Reaksi pengikatan atau penerimaan elektron. Dalam konsep redoks, peristiwa pelepasan elektron dinamakan oksidasi, sedangkan peristiwa penerimaan elektron dinamakan reduksi. Oksidator adalah zat yang menerima elektron.sedangkan reduktor adalah zat yang melepas. Reaksi redoks pada peristiwa perkaratan besi dapat dijelaskan dengan reaksi berikut:
Konsep redoks berdasarkan pelepasan dan pengikatan.
Terjadi pengikatan oksigen (oksidasi) dan pelepasan oksigen (reduksi). Reduksi adalah reaksi pengikatan atau penerimaan elektron. Konsep redoks berdasarkan pelepasan dan pengikatan. Besi dihasilkan reduksi bijih besi fe 2 o 3 dengan reduktor kokas (c) pada tanur tinggi.
 Source: kimiavegas.wordpress.com
Source: kimiavegas.wordpress.com
Terjadi pelepasan elektron (oksidasi) dan penerimaan elektron (reduksi). Oleh karena banyak reaksi redoks yang tidak dapat dijelaskan dengan konsep pengikatan oksigen maupun transfer elektron maka para pakar kimia mengembangkan konsep alternatif, yaitu perubahan bilangan oksidasi. Reaksi pengikatan atau penerimaan elektron. Untuk mencapai kestabilannya, atom mg harus melepaskan 2 elektron, sedangkan atom cl membutuhkan 1. Reaksi oksidasi pelepasan penerimaan elektron.
 Source: kimiavegas.wordpress.com
Source: kimiavegas.wordpress.com
Reaksi di atas menunjukkan terjadinya pelepasan dan pengikatan elektron, maka dapat disimpulkan sebagai berikut. Zn (s) + cu2+(aq) → zn2+(aq) + cu (s) reaksi keseluruhan adalah jumlah dari kedua setengah reaksi, yaitu setengah reaksi oksidasi dan setengah reaksi reduksi yang disebut reaksi redoks. Reaksi di atas menunjukkan terjadinya pelepasan dan pengikatan elektron, maka dapat disimpulkan sebagai berikut. Suatu reaksi kimia dikatakan sebagai suatu reaksi redoks jika: Besi oksida dapat direduksi dengan cara direaksikan dengan gas hidrogen, persamaan reaksinya:
 Source: materikimia.com
Source: materikimia.com
Zn (s) + cu2+(aq) → zn2+(aq) + cu (s) reaksi keseluruhan adalah jumlah dari kedua setengah reaksi, yaitu setengah reaksi oksidasi dan setengah reaksi reduksi yang disebut reaksi redoks. Oksidasi adalah peristiwa pelepasan elektron. Reaksi redoks pada peristiwa perkaratan besi dapat dijelaskan dengan reaksi berikut: Oleh karena banyak reaksi redoks yang tidak dapat dijelaskan dengan konsep pengikatan oksigen maupun transfer elektron maka para pakar kimia mengembangkan konsep alternatif, yaitu perubahan bilangan oksidasi. Terjadi kenaikan bilangan oksidasi (oksidasi) dan penurunan bilangan oksidasi (reduksi)
Situs ini adalah komunitas terbuka bagi pengguna untuk menuangkan apa yang mereka cari di internet, semua konten atau gambar di situs web ini hanya untuk penggunaan pribadi, sangat dilarang untuk menggunakan artikel ini untuk tujuan komersial, jika Anda adalah penulisnya dan menemukan gambar ini dibagikan tanpa izin Anda, silakan ajukan laporan DMCA kepada Kami.
Jika Anda menemukan situs ini baik, tolong dukung kami dengan membagikan postingan ini ke akun media sosial seperti Facebook, Instagram dan sebagainya atau bisa juga save halaman blog ini dengan judul contoh reaksi redoks sebagai pelepasan dan penerimaan elektron dengan menggunakan Ctrl + D untuk perangkat laptop dengan sistem operasi Windows atau Command + D untuk laptop dengan sistem operasi Apple. Jika Anda menggunakan smartphone, Anda juga dapat menggunakan menu laci dari browser yang Anda gunakan. Baik itu sistem operasi Windows, Mac, iOS, atau Android, Anda tetap dapat menandai situs web ini.